Totes les malalties que anomenem càncer, tot i la seva diversitat, tenen en comú una proliferació cel·lular anormal. Quan les cèl·lules deixen de dividir-se de manera ordenada, l’estructura i la funció dels teixits als quals pertanyen es veu afectada. Aquest desordre és l’origen de la malaltia, i de la mateixa paraula càncer —del grec karkínos o cranc—, que es refereix a les protuberàncies en les primeres lesions observades i que recordaven les potes d’aquest animal. També la paraula tumor deriva d’aquesta inflor –tumoris en llatí– causada per la divisió descontrolada, que pot ser benigna o maligna.
Avui sabem que en aproximadament un 70% dels càncers hi ha una desregulació del gen MYC, un gen que en condicions normals controla eficaçment centenars de gens implicats en el creixement ordenat de les cèl·lules.
Per això, quan aquest gen s’expressa de manera anòmala, pot desencadenar una proliferació cel·lular excessiva que no només impulsa el desenvolupament tumoral i la seva capacitat metastàtica, sinó que dificulta la resposta del sistema immunitari i afavoreix la resistència al tractaments actuals. D’aquí que comunament se’l coneix com a oncogen MYC.
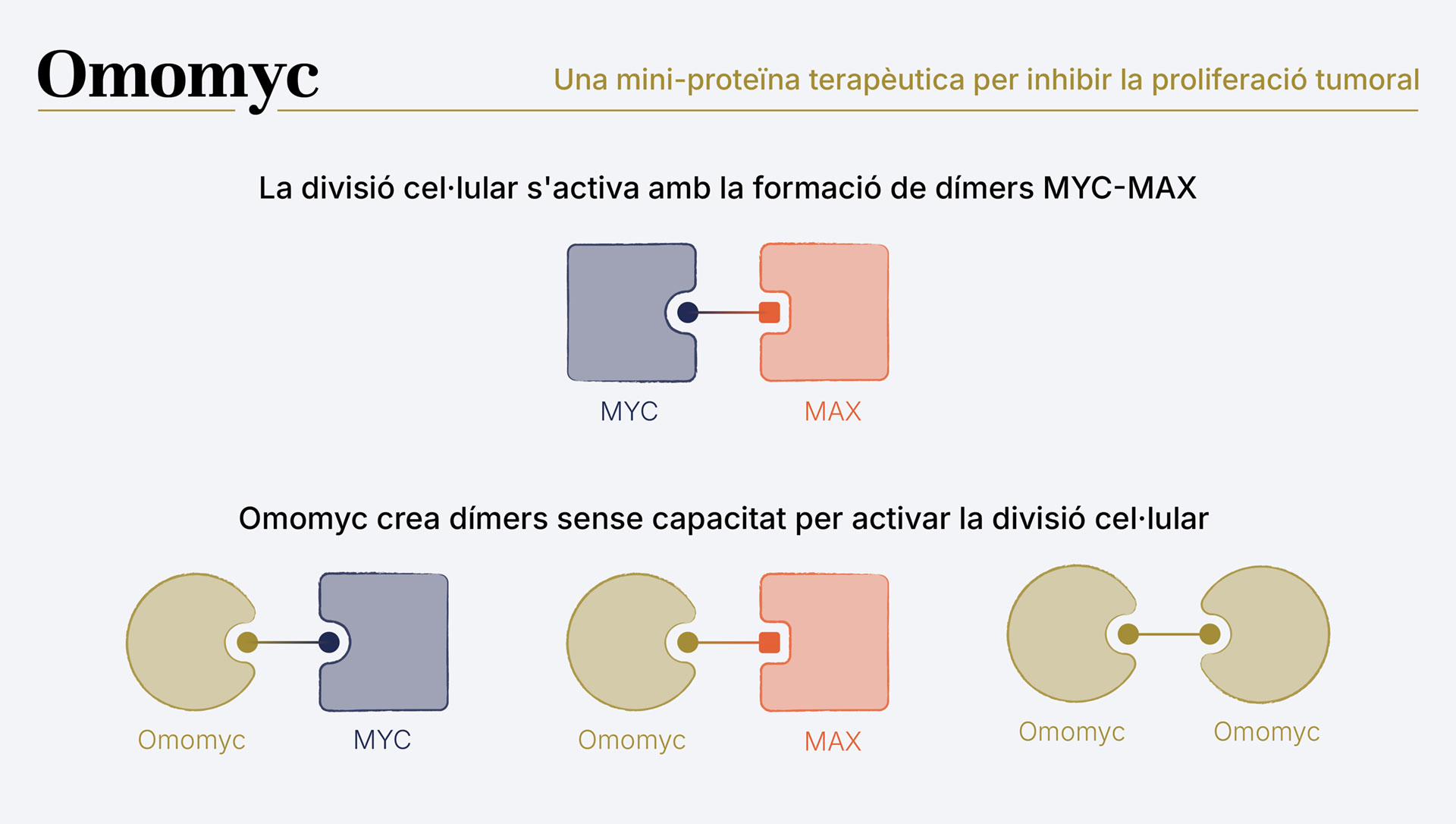
Durant molts anys, investigadors arreu del món han estudiat aquest oncogen com a diana terapèutica. L’oncogen MYC ha resultat ser un gen molt difícil de blocar, i són molts els que van arribar a pensar que no era abordable farmacològicament. Fins que una investigadora ICREA al Vall d’Hebron Institut d’Oncologia (VHIO), la Laura Soucek, va desenvolupar Omomyc: una mini-proteïna que pot inhibir l’activitat de MYC i que, administrada de manera segura, podria esdevenir una peça clau en el tractament de nombrosos tumors.
De moment, Omomyc s’ha provat tant en models preclínics com en un assaig clínic de fase 1, i en ambdós casos els resultats són prometedors: pot reduir la proliferació tumoral, disminuir la metàstasi i estabilitzar —o fins i tot regressar— tumors agressius com el melanoma o el càncer de pàncrees.
Ara bé, potser et preguntaràs per què encara no s’utilitza als hospitals. La resposta és que el desenvolupament de nous fàrmacs segueix procediments estrictes per tal de garantir-ne la seguretat i confirmar que realment milloren els tractaments existents.
Omomyc, que en la seva formulació clínica es coneix com a OMO-103, ha acabat amb èxit un assaig clínic de fase 1, destinat a avaluar la seguretat del fàrmac, amb 22 pacients amb tumors sòlids metastàsics que ja havien esgotat altres opcions terapèutiques. Malgrat l’avançat estat de la malaltia, la Laura i el seu equip van observar com en molts casos el tumor s’estabilitzava, amb durades que anaven des d’un mes fins a gairebé dos anys.
Gràcies a aquest assaig clínic, a més, els investigadors han pogut identificar biomarcadors rellevants que ajuden a predir en quins casos OMO-103 pot ser especialment eficaç, així com els processos metabòlics que afavoreix. En alguns pacients, per exemple, van detectar senyals associats a l’activació de la resposta immune antitumoral.
Ara, OMO-103 avança cap a una possible comercialització amb un assaig clínic de fase Ib específic per a càncer de pàncrees i en combinació amb tractaments estàndards, com la quimioteràpia. També han engegat un assaig clínic de fase 2 per a una monoteràpia en pacients amb osteosarcomes avançats, una malaltia rara que afecta especialment a nens i adolescents. A més, continuen les millores del fàrmac per a poder-lo provar en altres tipus de càncer i en altres estadis de la malaltia. Si els resultats continuen sent positius, les autoritats reguladores podrien aprovar la comercialització del fàrmac en pocs anys, potser abans d’acabar la dècada.